روش های تولید پر اکسید هیدروژن( آب اکسیژنه) :
روش های تولید پر اکسید هیدروژن( آب اکسیژنه) :
پر اکسید هیدروژن ، همچنین تحت نام آب اکسیژنه H2O2 معروف است که به مقدار کم در جو و در بعضی از گیاهان به وجود می آید. این ماده خاصیتی دارد که باکتری ها را از بین می برد لذا کاربرد زیادی به عنوان ضد عفونی کننده و میکروب کش دارد . در این مقاله به بررسی روش تولید پر اکسید هیدروژن می پردازیم.
خصوصیات پر اکسید هیدروژن(آب اکسیژنه) :
۱- پر اکسید هیدروژن مایع شیره مانندی است که بی رنگ و بی بو می باشد.
۲- دارای وزن مخصوص برابر ۱٫۴۶ و نقطه ذوب ۸۵ درجه سانتیگراد در حالت بدون آب است.
۳- این ماده با آب و الکل به هر نسبتی امتزاج پذیر است.
۴- پر اکسید هیدروژن یک ترکیب ناپایدار است . در اثر ماندن و در اثر حرارت تولید آب و اکسیژین می نماید.
۵- این ماده یک عامل اکسید کننده قوی می باشد.
کاربرد و موارد مصرف پر اکسید هیدروژن (آب اکسیژینه):
۱- به عنوان عامل اکسید کننده در بعضی از واکنش های آزمایشگاهی استفاده می شود.
۲- به عنوان نیروی محرکه رانش موشک به کار می رود.
۳- برای تعمیر و تجدید رنگ های حاوی سرب به کار می رود.
۴- به عنوان ماده سفید کننده جهت مو ، پشم ، عاج و بعضی از انواع چرم مورد استفاده قرار می گیرد
۵- به عنوان ضد عفونی کننده و میکروب کش جهت شستشوی زخم ها ، دندان ها و گوش ها مصرف می شود.
۶- پر اکسید هیدروژن به عنوان یکی از سفید کننده های مهم در منسوجات کاربرد دارد.
بررسی جایگاه صنعتی پر اکسید هیدروژن (آب اکسیژنه):
پر اکسید هیدروژن یک ماده شیمیایی بسیار با اهمیت است که کاربرد های متنوعی در صنایع ، داروسازی و پزشکی دارد. تقاضا جهت مصرف این ماده سیر صعودی دارد.
روش تولید پر اکسید هیدروژن (آب اکسیژنه):
پر اکسید هیدروژن را می توان به روش های مختلفی تولید نمود که عبارتند از:
۱- از پراکسید باریم و اسید سولفوریک
۲- از پراکسید سدیم و اسید سولفوریک
۳- از طرسق اکسیداسیون خود به خود
۴- روش الکترولینیکی
در بین همه این روش ها ، طرقه الکترولیز یک روش مدرن و تجارتی است. پر اکسید هیدروژن به وسیبه الکترولیز اسید سولفوریک ۵۰ درصد در یک سل دیافراگمی و تقطیر در خلا تولید می گردد. حاصل تقطیر محلول ۳۰ درصد پر اکسید هیدروژن خالص می باشد. اولین محصول الکترولیز پر سولفوریک اسید H2S2O8 می باشد که بعدا با آب وارد واکنش شده و هنگام تقطیر تولید پر اکسید هیدروژن می نماید. واکنش ذیل اتفاق می افتد.
H2SO4 <——-> H + HSO4
۲ HSO4 <—–> H2S2O8 + 2e
H2S2O8 + H2O <—> H2SO4 + H2O2
۲H + 2e —–> H2
تغلیظ هیدروژن پر اکسید (آب اکسیژنه)
عملیات تغلیظ پر اکسید هیدروژن خطرناک است زیرا ناخالصی های موجود مخصوصا مواد آلی ممکن است به عنوان کاتالیزور عمل نموده و باعث تجزیه شیمیایی و انفجار گردد. با این وجود ، با عملیات تبخیر دقیق و با احتیاط محلول بدست آمده فوق الذکر را توسط حمام آب تیجیحا تحت فشار پایین( کاهش فشار ) و با استفاده از تقطیر جز به جز تغلیظ می نمایند.
پر اکسید هیدروژین به طور قابل ملاحظه ای از آب کمتر فراریت دارد و آب از دست می دهد تا محلول ۳۰ درصد به دست آید . تغلیظ بیش از ۳۰ درصد مطلوب نمی باشد.
تغلیظ بیش از ۳۰ درصد:
به وسیله تقطیر تحت فشار پایین (کاهش فشار) در درجه حرارات زیر ۶۰ درجه سانتیگراد عملیات تغلیظ تا غلظت ۹۰ درصد ممکن خواهد بود. جهت تهیه محلول غلیظ و در نهایت پر اکسید هیدروژن خالص ، محلول ۹۰ درصد را سرد می کنند. تا میزان بلور های پر اکسید هیدروژن فراوان تر از محلول هنوز مانده گردد. بلور های را جدا سازی ، ذوب و آب می کنند که در نتیجه غلظت بیشتر به دست می آید.
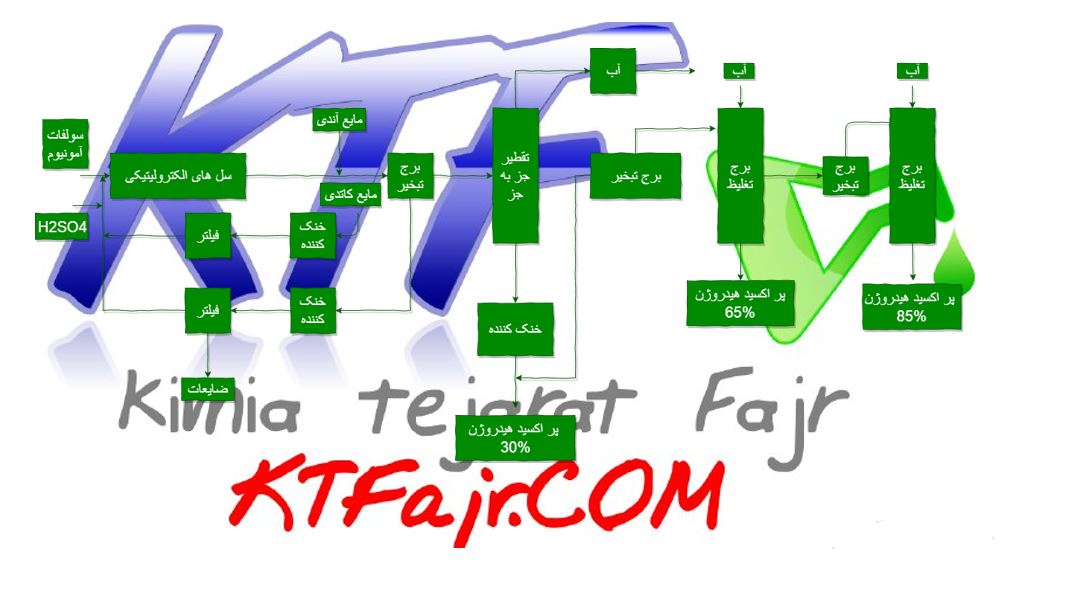
نمودار جربان تولید پر اکسید هیدروژن (آب اکسیژنه)
لیست تجهیزات و ماشین آلات :
۱- سل دیافراگمی
۲- ژنراتور دی سی
۳- برج تقطیر خلا
۴- بویلر ثانویه
۵- کندانسور جت
۶- کندانسور تبخیر کننده سطح
۷- پمپ خلا چند مرحله ای
۸- کمپرسور گاز هیدروژن
۹- مخزن ذخیره سازی گاز هیدروژن
۱۰ – مخازن ذخیره سازی پر اکسید هیدروژن
۱۱- مخزن ذخیره سازی اسید سولفوریک
۱۲- بویلر

مقدار لازم از هر ماده ی اولیه جهت ساخت هیدروژن پراکسید چقدر هست؟؟؟
برای بدست آوردن حدودی این میزان باید به پتنت های خارجی رجوع کنید
ولی مقدار دقیق با توجه به خلوص مواد مصرفی و شرایط محیط متفاوت است و با انجام آزمایشهای مختلف بدست می آید
سلام
آیا میشه در اکسید هیدروژن رو خریداری کرد
سلام
بله محصول در بسته بندی های مختلف قابل عرضه به بازار است.
با تشکر