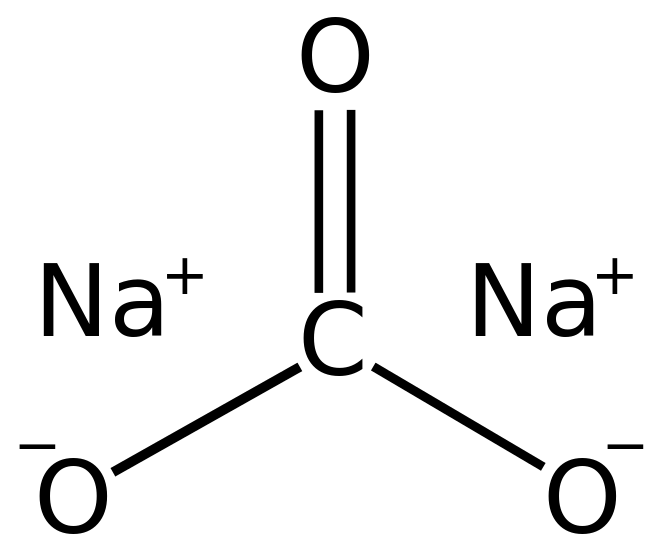
سدیم کربنات (sodium carbonate) – سودا اش(soda ash) – سودای شستشو (washing soda) – کریستال سودا (soda crystals) – کربنات دو سود(carbonate de sodium) – سودا مونو هیدرات(soda monohydrate) – نمک سدیم اسید کربنیک
تاریخچه:
سودا اش از لحاظ رتبه ، دهمین ترکیب و جزء معدنی پرمصرف در جهان است. و خدود 500 سال است که استفاده می شود.
مردم مصر در دوران باستان ، خاکستر سودا را از کف دریاچه های خشک بدست می آوردند. و یا از سوزاندن گیاهاهان دریائی که حاوی مقادیر زیادی سودا اش بود ، یدست می آوردند. این افراد برای کم کردن نقطه ذوب سیلیس و ماسه در تولید ظروف شیشه ایی از مخلوط سودا اش استفاده می کردند. رومی ها از ترکیبات آن که جوش شیرین می یاشد برای تولید نان و موارد داروئی استفاده می کردند.
خواص آزمایشگاهی کربنات سدیم:
۱- حالت فیزیکی: پودر خشک
۲- رنگ: پودر سفید تا خاکستری شامل تا ۹۹درصد سودا اش
۳- طعم: بدون طعم
۴- بو: بدون بو
۵- نقطه جوش: با حرارت دادن و خروج CO2 شروع به تجزیه میکند
۶- نقطه ذوب: در ۸۵۶ درجه سانتیگراد
۷- حلالیت: در آب حل می شود و در الکل اتانول نامحدود است.
دمای ۲۵ درجه سانتی گراد در ۱۰۰ گرم آب ۳۰٫۷ گرم از آن حل میشود
و حلالیت آن در آب در دمای ۰ و ۱۰ و ۲۰ و ۳۰ به ترتیب ۶ و ۸٫۵ و ۱۷ و ۲۸ درصد وزنی می باشد.
۸- دانسیته: ۲٫۵۴ g/cm3
۹- پایداری: تحت شرایط نگهداری توصیه شده پایدار است
۱۰- تجزیه: این ماده در مجاورت فلوئور در دمای معمولی تجزیه می شود
حدود دما ی ۴۰۰ درجه سانتی گراد با خروج گاز co2 شروع به تجزیه می کند
در دماهای بالاتر، وقتی حرارت داده می شود، بخارات سمی Na2o منتشر می شود.
۱۱- Ph: محلول های آبی آن به شدت قلیایی است . در ۲۵ درجه سانتی گراد و در محلول های ۱ و ۵ و ۱۰ درصد آبی آن ph به ترتیب ۱۱٫۳۷ و ۱۱٫۵۸ و ۱۱٫۷۰ دارد
کاربرد های صنعتی کربنات سدیم
کاربرد های خانگی کربنات سدیم

سدیم کربنات
سودا اش یکی از مواد خام برای تولید شیشه است . در حدود نیمی از سودا اش تولیدی در کل دنیا برای تولید شیشه استفاده می شود . این ماده همچنین برای تولید مواد تمیز کننده ، در متالوژی و صنعت شیمیایی ، برای تولید نوعی از کود های معدنی و همچنین پیگمنت ها استفاده می شود .
تولید سیسکویی کربنات :
تری سدیم هیدروژن دی کربنات ( سیسکویی کربنات) به فرمول ترکیبی NaHCO3و Na2CO3 است . ساختمان کریستالی شبیه سوزن دارد. و اصطلاح سیسکویی به مخلوط هم مولار از دو نمک اتلاق می شود که آب هیدراته سدیم کربنات در فرمول باقی می ماند و به شکل پودر به بازار عرضه می شود.
فرمول شیمیایی ترکیبNa3H(CO3)2 .2H2o را دارد. به صورت دو آبه دانسیته 2.112 گرم بر سانتی متر مکعب را دارد. حللالیت آن در دمای صفر درجه سانتی گراد 13 گرم و در دمای 100 درجه سانتی گراد 42 گرم به ازای 100 میلی لیتر آب است. به دلیل آن چیزی که به سمیت براکس به عنوان محصول تمیز کننده و پاک کننده مربوط می شود سیسکویی کربنات به عنوان جایگزینی برای برا کس در اروپا فروخته می شود و به عنوان یکی از منابع ویتامین E است که به صورت E500 شناخته شده است.
سیسکویی کربنات در حمامهای نمکی ، در استخرهای خانگی و عمومی ، به عنوان منبع قلیائی برای عملیات تصفیه آب استفاده می شود. همچنین به عنوان یک منبع عاری از فسفات به عنوان جایگزینی برای تری سدیم فسفات در تمیز کننده های حرفه ایی استفاده می شود .
به عنوان ته نشین کننده در آب های سخت و در حین نرم سازی استفاده می شود. و روش کار بدین ترتیب است که با املاح آب های سخت همچون کلسیم و منیزیم ترکیب می شود و به صورت رسوب ظاهر می شود که به راحتی قابل جداسازی هستند .
تولید شیشه :
کربنات سدیم به عنوان فلاکس برای سیلیس عمل می کند. تا بتواند نقطه ذوب مخلوط را در حدی پایین بیاورد که بدون نیاز به مواد خاص ، عملیات تولید انجام شود. ترکیب سودا و شیشه به آرامی در آب حل می شود ، بنابراین بایستی کلسیم کربنات به مخلوط مذاب اضافه کنیم تا شیشه را به صورت نامحلول در آوریم. بطری و شیشه پنجره ها با ذوب مخلوطی از کربنات سدیم و کلسیم کربنات و سنگ سیلیس (دی اکسید سیلیسیم ) تولید می شوند. وقتی این مواد حرارت داده می شوند ، کربنات به صورت دی اکسید کربن آزاد می شود. در این روش کربنات سدیم منبعی یرای اکسید سدیم است.شیشه سودا آهکی طی قرن ها عمومی ترین شکل از نوع شیشه بوده است. آن یک ورودی اساسی برای تولید شیشه های رو میزی بوده است.
نرم کننده آب :
آب سخت شامل اجزای تجزیه شده است .این اجزاء شامل کلسیم و منیزیم هستند. کربنات سدیم برای حذف موقتی و پایدار سختی آب استفاده می شود. در حالی که کربنات سدیم محلول در آب است و کربنات کلسیم و منیزیم نامحلول در آب هستند‚ ابن ماده برای نرم کردن آب با برداشتن یونهای کلسیم و منیزیم عمل می کند. در حین عملیات این بونها رسوب های جامد نامحلولی را تشکیل می دهند.
Ca+CO3→CaCO3
Ca (aq)+Na2CO3(aq)→CaCO3
و به طور مشابه
Mg (aq)+Na2CO3(aq)→CaCO3+2Na
یعد ازاین عملیات ‚ آب نرم می شود چرا که شامل هیچ بون کلسیم و منیزیمی نیست.
به عنوان ادتیو غذائی و پخت و پز:
سدیم کربنات چندین موارد ‚ کاربرد در آشپزی دارد. و کاربردهای منحصر یه فرد آن در صنعت غذائی به این دلیل است که درمقایسه با بی کربنات سدیم ‚ بازقوی تری است. در مقایسه با سود سوز آور باز ضعیف تری است. و در مقایسه با پتاس کمتر عمومی است.
کاربردهای متفرقه:
در صنعت بلوک و سفال و کاشی سرامیک و آجر به عنوان مرطوب کننده استقاده می شود . و نقش آن کاهش آب مورد نیاز برای اکستروژن خاک رس و دوغاب است. صنعت ریختگری به ان عامل چسبنده یا پیوند دهنده اطلاق می شود. باعث می شود . آلژینات مرطوب به ژل های آلژینات بجسبد. هم جنین در حمبر دندان استفاده می شود. که نقش آن عامل فوم کننده و ساینده است. و به طوز موقتی pH دهان را اقزایش می دهد. هم چنین در دباغی و فرآوری پوست حیوانات کاربرد دارد.
روش اندازه گیری مقدار سدیم کربنات در شوینده ها به روش تیتراسیون:
تیتراسیون از دبریاز روشی بسیار عملی و ساده برای اندازه گبری های آزمایشگاهی بوده است. در این روش مقدار سدیم کربنات که در شوینده ها حدود 16 درصد در شوینده های خانگی است اندازه گبری می شود.
تمونه به صورت محلول در می آبد در حالی که سدیم کربنات در نمونه ‚ بوسیله کلرید یاریم جذب می شود. در ادامه کربن دی اکسید و اضافه باریم ‚ بوسیله EDTA تیتر می شود.
با استفاده از سولفوریک اسید 30 درصد ححمی ‚ کربنات سدیم در کلرید باریم جذب می شود . و از این طریق کربن دی اکسید آزاد می شود. رسوب کربنات یاریم فیلتر می شود و اضافه یون باریم در محلول با استفاده از معرف اریوکروم بلک تی با استفاده از EDTA تیتر می شود. بعد از این مرحله معرف و کربنات سدیم محاسیه می شود.
زمان مورد نیاز برای آنالیز نمونه 11.5ساعت است. و با این روش تا 96.9 درصد ورنی کربنات بازیافت می شود. باید توجه داشت از این روش کربنات محلولهای سدیم کربنات ‚ را هم می توان اندازه گرفت.
دو نوع سودا اش وجود دارد : کربنات سدیم سبک ( light soda ash ) کربنات سدیم سنگین (dense soda ash )
تفاوت عمده کربنات سدیم سبک و سنگین در چیست؟
تفاوت های عمده توع سبک و سنگین در دانسیته و چگالی توده آن است . به طوری که یک تن سودا اش سبک حجم بیشتری نسبت به یک تن سودا اش سنگین دارد . ولی سایر خواص شیمیایی آن ها کاملا مشابه است . نوع سفارشی خریدار به تکنولوژی استفاده و اولویت های فرایند تولید بستگی دارد . دانسینه نوع سبک 700 گیلوگرم برای هر متر مکعب است. دانسیته نوع سنگین 900 گیلوگرم برای هر متر مکعب از حجم است.
تفاوت دیگر مربوط به قیمت این دو است . نوع سبک معمولا ارزانتر از نوع سنگین است.
روش تولید کربنات سدیم سبک و سنگین :
سودا اش به طور عمده بوسیله روش آمونیاک قلیائی تولید می شود. که مواد اولیه نمک و سنگ آهک را استفاده می کند. سودا اش لایت بوسیله سنتز مواد شیمیائی تولید می شود. و سودا اش سنگین بوسیله روش جامد و فاز آب تولید می شود.
سودا اش سنگین بوسیله روش قلیائی طبیعی تولید می شود. در حالی که قلباهای طبیعی به عنوان مواد خام هستند وبوسیله روش تبخیر یا روش کربونیزاسیون تولید می شوند.
انواع کربتات سدیم های قابل عرضه در بازار ایران
کربتات سدیم تولیدی سمنان
کربنات سدیم سرخه سمنان (ساکو )از سال 1401فعالیت خود را آغاز نموده است. در سال 1385با ظرفیت روزانه 500 تن به بهره برداری رسید.نامهای دیگر این شرکت SIG(Sahand Industrial Group) و است. این شرکت علاوه بر توزیع در شبکه داخل کشور‚صادرات به کشورهای همسایه هم دارد . طوری که به بیش از 15 کشور دیگر محصولات خود را صادر می کند. کشورهای عمان ‚امارات متحده عربی ‚هندوستان ‚ کویت و مصر ‚ عربستان سعودی ‚سوریه ‚ عراق ‚ ارمنستان ‚ نرکیه ‚ ایتالیا و پاکستان و .. از جمله این کشورها هستند . بسته بندی محصولات این کارخانه در کیسه های 40 کیلویی و 50 کیلوئی و جانبو بک های 1تنی متغیر
است.
عمده مصرف کننده های کربنات سدیم سنگبن کارخانجات بلور و شیشه هستند . در عوض مصرف کننده های نوع سبک ‚عمدتا کارخانجات شوینده (حانگی و صنعتی )کاشی و سرامیک و . هستند .
آنالیز کربنات سدیم سبک سمنانsemnan light soda ash
semnan dense soda ash آنالیز کربنات سدیم سنگین سمنان
کربنات سدیم تولیدی شیراز
پتروشیمی شیراز جزء اولین کارخانجاتی بود که کار تولید کربنات های سبک و سنگین و محصولات دیگری از جمله کودهای ازته و آمونیاک و…را شروع کرد. کیفیت کربنات های تولیدی این کارخانه بسیار بالا بود و عناصر مزاحم خیلی کمی از جمله آهن و …داشت و کربنات تولیدی آن بسیار سفید بود و در حقیقت استاندارد محصول بالائی داشت.تیراژ تولید هم روزانه بالغ بر 500 تن بود. ولی متاسفانه به دلیل آلودگی هایی که برای محیط زیست ایجاد می کرد مجبور به تعطیلی واحد کربنات سدیم سبک و سنگین شد . به دلیل اینکه کربنات سدیم شیراز در بازار ایران موجود نیست از ارائه مشخصات فنی و ارائه آنالیز آن خودداری می کنیم.
کربنات سدیم تولیدی مراغه
کارخانه کربنات سدیم کاوه‚ در شهرمراغه استان آذربایجان شرقی کار خود را با تولید نوع سبک و سنگین آغاز کرد و تولید خود را تا روزانه 1000 تن افزایش داد. صنعت شیشه و بلور ‚صنایع پاک کننده اعم از خانگی و صنعتی ‚ تصفیه اب و فاضلاب و پتروشیمی ها و ..ازجمله مشتریان عمده این کارخانه هستند. کم کم این کارخانه شروع به تولید جوش شیرین (بی کربنات سدیم ) برند ساچی کرد. در سال 1384 فاز دوم این کارخانه در فیروز آباد استان فارس راه اندازی شد.که قرار است تا روزانه 3000 تن کربنات سدیم تولید کند. محصول تولیدی مراغه این واحد با نام کاوه سودا به بازار عرضه می شود. و محصول فیروزآباد با نام ساچی (SACHI)به بازار عرضه می شود.
کربنات سدیم ازبکستان
محصول تولیدی ازیکستان در دونوع سبک و ستگین به بازار ایران وارد شده است.بسته بندی کیسه 45 کیلویی و جانبوها 1تنی هستند.کربنات ازبک و یا کربنات ازبکستان کیفیت پایین تری نسبت به نمونه مشابه ایرانی دارد.
ایمنی در کارحانجات کربنات سدیم
کارخانه های کربنات چون کارخانه های مادر بوده و حیات کارخانجات دیگر به آنها وابسته است بایستی از امنیت بالایی برخوردار باشند.چرا که وقفه در کار تولید آنها ‚ کارخانه های زیادی را با مشکل مواجه می کند .
-امنیت در بخش عمل آوری و تامین آمونیاک
آزاد شدن آمونیاک بسیار سمی برای مجموعه و کارگران و محیط زیست است.آمونیاک داخل بسترهای آبی نفوذ می کند و باعث بالا رفتن pH آب می شود واثر معکوس در اکوسیستم آبزیان دارد. قبلا در یک تجربه مشابه ‚ مقدار زیادی ماهی مرده در نواحی آبی آلوده به آمونیاک ‚ کشف شده است. بررسی یر روی منابع آلودگی های محتمل و سناریوهای موجود انجام گرفت. سرعت باد و جهت باد ‚ برروی نواحی آلوده در معرض قرار گرفته بسیار موثر بودند.به هر حال عموم مردم بایستی نسبت به خطر در معرض قرار گیری با نشت گاز آمونیاک در محیط اطراف پیرامونی تا مسافت ها ‚ آشنا باشتد.
دلایل انفجار در کارخانه کربنات سدیم
دلایل زیادی وجود دارد که انفجار مخزن آمونیاک تحت فشار را باعث می شوند.جنس نامناسب ورق مخازن ‚ خوردگی داخلی و خارجی مخازن‚ خرابی شیرهای کنترل کننده ‚ افزایش فشار و دما همه می توانند موثر باشند. خطای انسانی هم می تواند موثر باشد.به هر حال نتایج نشان داد که به دلیل خطاهای عملیانی ‚ مخازن حاوی آمونیاک بیش از حد تحت فشار بوده اند. فراتر از این ‚ هیچ لایه محافظی وجودنداشت تا آمونیاک های آزاد شده را جذب کند و اثرات آن را به حداقل برساند.
به دلیل حساسیت بالا در کارخانه های تولیدی کربنات ‚ بایستی تقویت امنیت کارخانه به شدت انجام شود . و دسترسی پرسنل غیرمجاز در مناطق حساس محدود شود. و خرابکاری های عمدی جلوگیری شود. و برای جلوگیری از حوادث مشابه ‚ تمامی حوادث ریشه یابی شود.
جایگزین های کربنات سدیم:
ماشین لیاسشوئی
سوداش که برای تولید مواد شوینده و مکمل های مواد شستشوی لباس استفاده می شود سختی آب را از بین برده و به از بین بردن لکه ها کمک می کند. جایگزین آن در این مورد سدیم بی کربنات یا جوش شیرین است. روش دیگربجای استفاده از جوش شیرین ‚ سرکه سفید است. سرکه وترکیبات آن به طور طبیعی سختی آب رااز بین می برد و مواد شیمیائی موجود در شوینده را که باعث واکنش های نامطلوب می شود خنثی می کند. در حالت عادی حدود 2فنجان سرکه سفید را در چرخه آب کشی اضافه کنید. برای لیاسهای تمیزتر حدود نصف فنجان سرکه اضافه کنید.
شستشوی فولاد ضدزنگ
کربنات سدیم برای شستشوی فولاد ضدزنگ و ظرفهای نقره ایی و قابلمه و سینک ظرفشوئی و وان حمام استفاده می شود. فولاد ضدزنگ ‚ فلزی مقاوم است اما در برابر خوردگی آسیب پذیر است. و ضروری است که تمیز کننده مناسبی برای آن استفاده شود. برای شستشوی معمولی بجای کربنات سدیم از جوش شیرین استفاده کنید. برای تمیز کردن سطخی و اثر انگشت از استون استفاده کنید.برای جایگزین های کربنات سدیم در تمیز کردن زنگ و اثرات خوردگی (Corrosion) از 9قسمت آب گرم و 1قسمت اسید نیتریک استفاده کنید.
ثابت کردن زنگ پارچه
صنعت نساجی جهت تثبیت رنگ پارچه ‚ نباز به سودا اش دارد که رنگ و pH حمام های نساجی را کنترل می کند. یک جایگزین مناسب برای سودا اش در این مورد ‚ سیلیکات سدیم است که آب شسشه نامیده می شود. تثبیت الیاف رنگ شده با اشیاع آنها در محلول سیلیکات سدیم و سپس شستن کامل با آب دیونیزه انجام می گبرد.
فرآوری کربنات سدیم از جوش شیرین :
سدیم کربنات یا جوش شیرین فرمول عمومی NaHCO3 رادارد. زمانی که به کربنات سدیم دسترسی نداشتید و یا در آزمایشگاه برای تولید آن ‚ بکینگ سودا یا سدیم بی کربنات را در 200درجه فارنهایت به مدت یک ساعت در کوره خرارت دهید. کربن دی اکسید و آب خارج شده و سدیم کربتات باقی می ماند . این همان سودا اش است. واکنش شیمیائی به قرار ذیل است:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(g)
سودا اش که بدست می آید به آسانی آب را جذب می کند و به شکل هیدرانه در می آید. در صورت لزوم شما می توانید سودا اش خشک را در ظرفهای سیل شده به همراه یک ماده جاذب مثل سیلیکاژل ذخیره کنید تا رطویت نگیرد و هیدراته نشود. در خقیقت به شکل خشک بماند. با حتی می توانیدآن را به خال خود رها کنید تا به شکل هیدراته در آید.
گرچه سدیم کربنات نسبتا پایدار است‚ در مجاورت هوا می تواند به کندی تجزیه شود تا اکسید سدیم و کربن دی اکسید را شکل دهد. واکنش تجزیه می تواند با حرارت سودا اش به 851 درجه سانتی گراد ‚ شتاب داده شود.
سودا اش و سدیم بی کربنات ‚ مولکولهای مشابه دارتد. تفاوت در مقدار مولکهای آبی است که فرمول را در بر گرفته است .
ساخت محلولهای کربنات سدیم :
ساخت محلولهای کربنات یا با غلظت های مشخص صورت می گیرد که به صورت درصد جرمی جزء حل شده صورت می گیرد. مثلا محلول 5 درصد. با در شکل مولاریته بیان می شود. که در این صورت به عنوان تعداد مولهای کربنات در 1لیتر محلول بیان می شود.
وقتی سدیم بی کربنات را در دمای بالای 80 درجه سانتی گراد حرارت می دهیم ‚ سدیم بی کربنات به سدیم کربنات و کربن دی اکسید و بخار آب تبدیل می شود. هر دو مول سدیم بی کربنات ‚ 1مول سدیم کربنات بعلاوه گاز دی اکسید کربن و آب می دهد. پودر سدیم بی کربنات به نظر می رسد در موقع حرارت دادن جمع شود با شیرینگ شود. حرارت دادن سدیم بی کربنات را داخل ظروف شیشه ایی تمیز یا تابه آلومینیومی انجام دهید.
برای ساخت سدیم کربنات با درصد جرمی مشخص از فرمول درصد جرمی در حجم تقسیم بر نفاضل جرم از 100 استفاده کنید . به عنوان مثال مقدار سدیم کربناتی که برای محلول 12 درصدبا حجم آب 350 میلی لیتر نیاز است ازحاصل تقسیم (350*12) بر (12-100) به دست می آید که عدد 47.73 گرم به دست می آید. البته اگر 12 را در 0.35 ضرب می کردید و تقسیم بر 350 می کردید عدد 0.12 بدست می آمد. ولی باید توجه داشت در این صورت باید جرم آبی کمتر از 350استفاده می کردیم. یعنی مجموع کربنات و آب 350 گرم می شد.
ساخت کربنات بامولاریته مشخص :
برای ساخت مقدار جرم کربنات مورد نیاز ‚ مولاریته را در حجم محلول به لیتر و عدد مولاریته که همان 106 هست ‚ ضرب کنید. مثلا مقدار جرم کربنات مورد نیاز برای ساخت 300 میلی لیتر محلول 0.2 نرمال از ضرب عدد 0.2 در 0.3 در 106 بدست می آید . جواب عدد6.36 گرم است.
برای ساخت محلول مقدار 6.36 گرم را وزن کنید . 20 تا 30 میلی لیتر کمتر از حجم تهایی آب به ظرف شیشه ایی مثل بشر اضافه کنید . کربنات را داخل ظرف شیشه ایی یریزید. در این مثال ما کار را با 270 تا 280 میلی لیتر آب شروع کنید. با یک به همزن محلول را کاملا به هم بزنید .تا نمک کامل حل شود . محلول را با استفاده از آب ‚ داخل بشر یا برای دقت بیشتر داخل استوانه مدرج به حجم نهائی برسانید. 300 میلی لیتر کربنات 0.2 مولار آماده شده است.
نگهداری و انبارداری کربنات سدیم (Packaging and Maintenance) :
در موقع انبارداری بایستی از برخورد با پوست ‚ چشم و یا لباس اجتناب شود. بعد از آلوده شدن دست با این محلول بایستی به طور کامل با آب شستشو شود. در محلهای مخصوص که تگهداری می شود هیچ خطر آتش گبری احتمالی ندارد چرا که خود خاموش کننده آتش است. در جای سرد و خشک و به خوبی تهویه شده و به دور از مواد ناسازگار مثل اسیدها بایستی نگهداری شود.
حمل و نقل کربنات سدیم بایستی از طریق کامیون و کشتی و در بیگ بگ و یا پالت های بسته بندی شده انجام گیرد.
این ماده بایستی در کیسه های 50 کیلویی دو لایه و یا یک لایه لمینت شده و یا جانبو های 1تنی نگهداری شود. وقتی این ماده در مجاورت هوای آزاد قرارگیرد کریستالهای آن آب از دست می دهند و به شکل پودر سفید غیر شفاف و مونوهیدرات در می آیند. از لحاظ انبارداری حداکثر 3 عدد جانبو 1تنی روی هم قرارگیرد. و کیسه های پنجاه کیلویی حداکثر پانزده ردیف روی هم چیده شود. در غیر این صورت فشار زیادی برروی ردیف های پایینی کربنات وارد می شود.